一文了解海水制氢技术路线及其难点
2022-02-28 10:56 来源:能源星球 点击:888
水是一种充足的自然资源,其约占地球表面的71%。其中,海水占地球全部水量的96.5%,与淡水不同,其成分非常复杂,涉及的化学物质及元素有92种。
海水中所含有的大量离子、微生物和颗粒等杂质,会导致制取氢气时产生副反应竞争、催化剂失活、隔膜堵塞等问题。为此,以海水为原料制氢形成了海水直接制氢和海水间接制氢两种不同的技术路线。
海水直接制氢的路线主要通过电解水制氢或光解水制氢方式制取,全球主要研究机构有中国科学院、法国国家科学研究中心、日本东北工业大学、北京化工大学、印度科学工业研究理事会、美国休斯敦大学等;
海水间接制氢则是将海水先淡化形成高纯度淡水再制氢,即海水淡化技术与电解、光解、热解等水解制氢技术的结合。
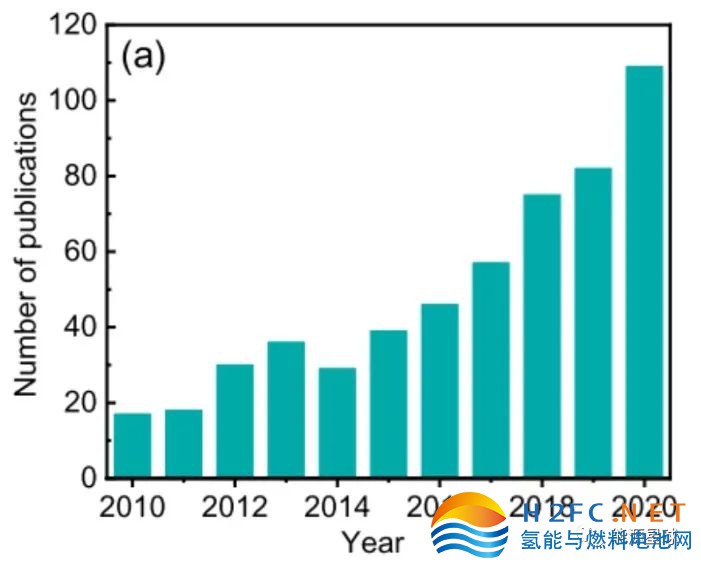
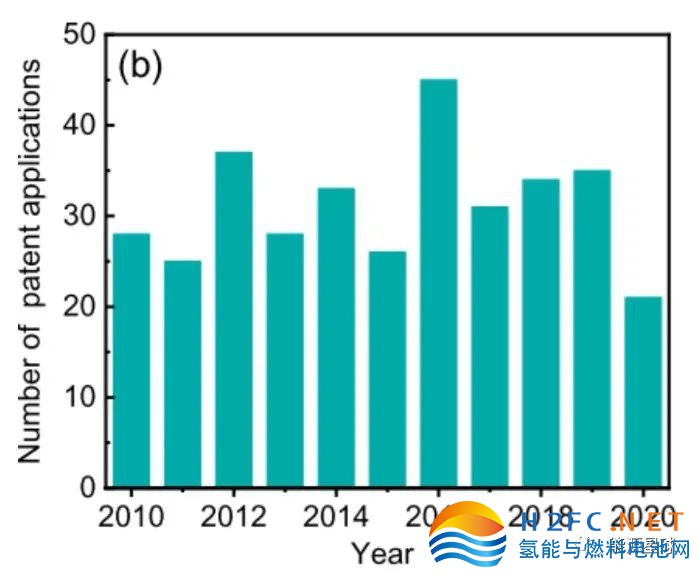
过去的几十年里,海水电解的研究取得了显著的进展(图1),发表了700多篇论文,340多项专利,得到数百万美元的研究资金。


图1:(a) 每年检索“海水分解”题目时,摘录的出版物数目;(b)在Patsnap数据库中搜索标题、摘要或权利要求中“海水”和“电解”等主题时,每年在Patsnap数据库中发现的专利申请数量。
电解水技术商业上存在的两种电解技术是碱性电解和质子交换膜(PEM)系统。碱性电解是一种成熟的商业技术,但在上世纪70年代天然气和SMR用于氢气生产时,这些电解槽几乎全部退役。
碱性电解槽的特点是避免了珍贵的催化剂,资本成本更低。而碱性电解系统在高效率(——55-70% LHV)、低电流密度(<0.45 A/cm²)和低操作压力(<30 bar)会对系统和制氢成本产生副作用。
此外,碱性电解槽的动态运行(频繁启动和变化的电源输入)可能对效率和气体纯度产生负面影响。
PEM电解是由Grubb在50年代早期首创的,通用电气公司在60年代领导开发,以克服碱性电解的缺点。PEM系统以纯水作为电解液,避免了碱性电解液中必需的腐蚀性氢氧化钾电解液的回收和循环。
到目前,由于PEM系统的紧凑设计,高系统效率,快速响应,动态操作,低温和在高压下产生超纯氢的能力,PEM在过去几年中电解槽堆成本大幅度降低,预计到2030年将成为可持续制氢的主导技术。
海水电解既可以通过氯氧化法生产氯,也可以通过水氧化产生氧。尽管氯是一种有价值的化学品,但不断增长的氢市场生产的数量将远远超过全球对Cl₂的需求。因此,研究选择性析氧的阳极催化剂是目前的主要挑战。
此外,海水中存在碳酸盐和硼酸盐离子,但它们的平均浓度太低,无法维持高电流密度。再者,由于海水本质上是一种非缓冲电解质,在电解过程中会导致电极表面附近的pH值发生变化(高达5-9个pH单位),导致盐沉淀、催化剂和电极降解其他离子、细菌、微生物和小颗粒的可能性,这些限制了催化剂和膜的长期稳定性。
因此,在达到工业级的电流密度的前提下,大多数报告使用了海水与硼酸盐缓冲液或KOH等添加剂。
尽管在直接电解海水这项技术上投入了大量资源和努力,但直接海水分离技术仍处于起步阶段,距离商业化还很遥远。
海水直接电解制氢技术
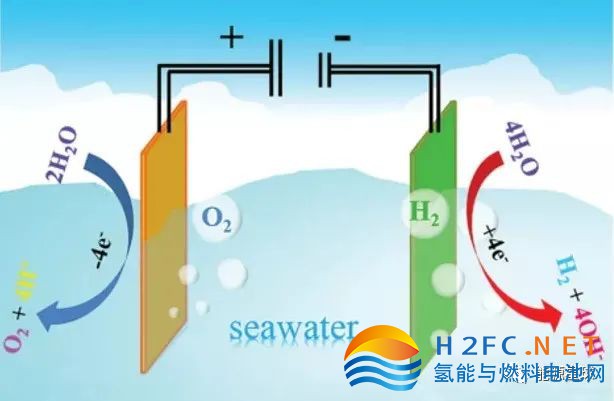
海水电解反应包括阴极析氢反应(Hydrogen Evolution Reaction,HER)和阳极析氧反应(Oxygen Evolution Reaction,OER)两个半反应(图2:电解海水制氢)。

图2
理论上同时驱动OER和HER的最小电压为1.23V,但是,在实际电解过程中需要额外的电位去激活和克服原始反应能垒,即过电位(η)。
因此,尽可能地降低水电解的过电位、降低能耗是发展电解制氢的关键,而加入催化剂可以降低过电位,提高反应速率。
在海水电解制氢过程中,对于HER,天然海水中存在各种溶解的阳离子(Na+,Mg2+,Ca2+等)、细菌/微生物和小颗粒等杂质。
这些杂质可能会随海水电解过程的进行而产生Mg(OH)₂、Ca(OH)₂沉淀物覆盖催化剂活性位点,从而使催化剂中毒失去活性。
对于阳极来说,OER是一个复杂的四电子质子转移反应,反应动力学缓慢,需要更高的过电位。
而海水中的高浓度氯离子带来的析氯反应(Chlorine Evolution Reactions,ClER)和次氯酸盐的形成都是二电子反应,与OER反应相比,反应动力学较快,因此会干扰OER并与之竞争,进而降低转化效率。
因此,开发具有高活性、高选择性的海水电解催化剂,对于避免海水中离子及杂质的影响至关重要。在国内外海水电解制氢方面,目前研究主要围绕HER催化剂、OER催化剂、双功能催化剂以及电解系统等开展。
1、阴极反应
对于阴极析氢反应(HER),直接海水裂解中最具挑战性的问题是天然海水中存在各种溶解的阳离子(Na+,Mg2+,Ca2+等),细菌/微生物和小颗粒等杂质。
这些杂质会随海水电解过程的进行阻塞电极,进而毒害或加速电解系统中电极/催化剂的老化,导致耐久性变差。
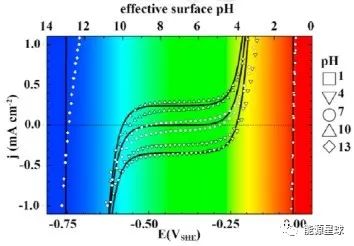
具体来说,随着电解电流密度的增加,电极表面局部酸碱度会急剧变化(图3:在H2饱和、无缓冲的pH1——13溶液中,通过循环伏安法获得的电流密度-表面酸碱度关系),因此可能导致Ca(OH)₂和Mg(OH)₂沉淀的形成,并阻塞阴极活性位点。

图3
为了解决该问题,目前的海水电解系统需要一种缓冲溶液或添加剂来稳定酸碱度波动。除此之外,设计合适的电解槽和隔膜等其他策略也有可能克服这一挑战。
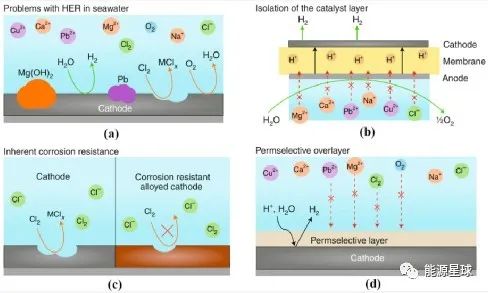
此外,取决于所施加的电解电势,海水电解过程中还可能发生涉及金属离子(如Na+,Cu2+,Pb2+)在阴极的竞争反应(图4:提高HER催化剂在海水中长期稳定性的挑战和潜在解决方案 a)。因此,抑制这些电化学过程对于海水中HER电催化剂的设计至关重要。
在这方面,采用合适的隔膜将催化剂与海水中的金属离子分离(图4:提高HER催化剂在海水中长期稳定性的挑战和潜在解决方案 b)、开发具有耐腐蚀性或选择性的催化剂(图4:提高HER催化剂在海水中长期稳定性的挑战和潜在解决方案 c),或使用如附着在催化剂上的选择性渗透阻挡层(图4:提高HER催化剂在海水中长期稳定性的挑战和潜在解决方案 d)等,被认为是提高HER电催化剂在海水中的长期稳定性的潜在解决方案。

图4
铂系金属被认为是HER基准电催化剂,在酸性、碱性和中性条件下均表现出最好的性能。但是,在海水电解过程中,其HER性能与在淡水电解质中的表现相差甚远。
另外,贵金属的稀缺和高成本极大地阻碍了其大规模应用。因此,在实际应用中,在保持高活性的同时减少铂的使用至关重要。
Yang Fengning等通过两步法制备Pt/Ni-Mo析氢催化剂,在113mV的过电势下模拟海水和工业条件,可在碱性溶液下稳定运行超过140小时,盐水(1M KOH+0.5 M NaCl)中达到2000 mA/cm2的电流密度,是迄今为止的最佳性能,并能够实现700cm²大面积制备。
除贵金属催化剂以外,探索廉价、高效和稳定的电催化材料是海水电解制氢的重要方向。过渡金属的催化活性被认为仅次于Pt族金属,而且价格便宜,其中Ni被认为是最有前途的催化剂之一。
一些研究人员制备了基于Ni的合金催化剂Ti/NiM(M=Co、Cu、Au、Pt),在HER中表现出显著的活性,但新型镍基催化剂还存在稳定性不足的问题,这是其应用的潜在障碍。
此外,非贵金属HER催化剂还包括过渡金属氧化物和氢氧化物、过渡金属氮化物(TMNs)、过渡金属磷化物(TMPs)、过渡金属硫族化物、过渡金属碳化物、过渡金属杂化物等。
TMPs因含量丰富、活性高和稳定性良好被用于海水HER。Lv Qingliang等报道了一种多孔的PF-NiCoP/NF析氢催化剂,在天然海水中具有高活性和持久性,且在287mV过电势下可达到10 mA/cm2的电流密度,优于商业化的Pt/C(20wt%),其研究认为三维形貌、空穴结构和导电基板提高了比表面积、电子转移和活性位点,从而有利于H2释放。
2、阳极反应
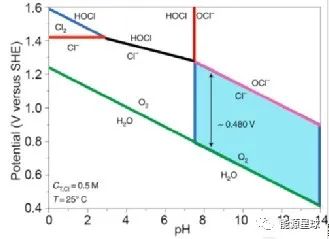
对于阳极来说,海水中含有大量电化学活性阴离子(如Cl-)会干扰阳极OER并与之竞争。Strasser等人对阳极海水电解及其局限性进行了深入的分析,他们得出了OER和氯化物相关的Pourbaix图(图5)。

图5:天然海水模型中OER和氯化物相关的Pourbaix图
如图5所示,析氯反应(ClER)和次氯酸盐的形成都是二电子反应,与OER四电子反应相比,这在动力学上是有利的,因而导致通常观察到的OER过电位比ClER高。
因此,开发对OER具有高选择性的电催化剂,对于避免海水直接电解过程中的ClER和次氯酸盐的形成至关重要。
用于从盐水中生产氢气的现有方法中还存在一些其他的效率低下问题。特别是,在无缓冲的溶液中的标准电解使得盐水产生氧(低于——2.25V)。
但是,在高于——2.26V时会产生氯。在阳极产生的任何氯立即水解,其还产生H+。随着阳极酸性增强,氯化合物在阳极优先进行氧化,从而形成氯气Cl₂,其为腐蚀性物质。Cl₂还与水反应形成次氯酸(HOCl)。
该过程中,溶液的酸性增加会腐蚀电极材料,要求其被更换,并导致溶液有毒,使得危险化学品的处理变得必要。
长久以来,高析氧活性的电催化剂通常是IrO2和RuO2等贵金属催化剂,然而这两种元素的稀有性决定了发展储量丰富的过渡族OER高活性催化剂的必要性。
由于OER复杂的四电子转移过程呈现反应动力学缓慢的特征,为应对ClER与OER竞争这一挑战,针对OER的选择性海水电解提出了三种主要策略,即碱性设计原理、具有OER选择性位点催化剂和Cl-阻挡层。
碱性设计原理主要基于热力学和动力学考虑,可以最大化OER和ClER之间的热力学电势差,从而保证对OER的高选择性。过渡金属氧化物和氢氧化物因引入氧空位,在碱性水中具有效活性位点,从而对OER具有良好的电催化性。
此外,通过掺杂Mo、Co、Fe、Ni、Mn或增加活性位点,可以提高OER的选择性。Yun Kuang等将硫化镍(NiSx)生长在泡沫镍上,又在硫化镍外电沉积一层NiFe-LDH层状双金属氢氧化物,形成多层电极结构。
其中泡沫镍起到导体的作用,NiFe-LDH为催化剂,中间硫化镍会演变成负电荷层,由于静电相斥而排斥海水中的氯离子,从而保护了阳极。
正因为这种多层设计,阳极可以在工业电解电流密度(0.4-1A/cm2)下运行1000小时以上。但是,该研究尚存在诸多待研究的工程细节,实现规模化、工业化需要进行放大实验。
3、双功能催化剂
设计具有较高活性和持久性的HER和OER双功能电解催化剂仍具有挑战。尽管碱性介质中存在不同类型的双功能水电解催化剂,如可对电子学性质和形貌进行必要改变的金属硫族化合物、氮化物、氧化物和磷化物,但其中可在海水中直接电解的还很少。
2020年,Wu Libo等通过“原位生长-离子交换-磷化”三步合成方法制备了双金属异质磷化物Ni2P-Fe2P,是一种具备了析氧反应(OER)和析氢反应(HER)双功能的催化剂,实现了对海水的高效稳定全分解产氢,在2.004V电压下全解水系统可达到500mA/cm2的电流密度,并且能稳定运行38小时以上。
4、电解系统
从应用角度来看,除了开发稳定高效的催化剂外,还必须设计合适的高性能、低成本海水电解槽。
目前,碱性水电解槽(AlkalineWater Electrolysers,AWE)和质子交换膜水电解槽(Proton Exchange Membrane Water Electrolyser,PEMWE)两种低温(<100℃)电解槽在商业市场较为成熟;
另外还有低温的阴离子交换膜水电解槽(AnionExchange Membrane Water Electrolyser,AEMWE)和高温水电解槽(High-Temperature Water Electrolysers,HTWE)两种新兴技术,其中高温电解包括质子导电陶瓷电解(150——400℃)和固体氧化物电解(800——1000℃)。
这些电解槽直接用来电解海水时,海水复杂的天然成分会对电解产生影响。其中主要问题是离子交换膜的物理或化学堵塞和金属组件的腐蚀,例如海水中的Na+、Mg2+和Ca2+离子会降低HTWE和PEMWE质子交换膜的性能;
Cl-、Br-、SO42-等阴离子又会对AEMWE、AWE和HTWE的膜性能产生不利影响。因此,开发稳定的隔膜是海水直接电解面临的重要挑战。
研究认为采用超滤、微滤对天然海水进行简单过滤,可以很大程度上解决固体杂质、沉淀物和微生物造成的物理堵塞。
LiuZhao等基于固体氧化物电解技术尝试了在高温下进行海水电解制氢,在未使用贵金属催化剂的条件下,以200mA/cm²的电流密度进行了420h的长期恒流电解,产氢速率为183 mL/min。
在不回收高温废气的前提下,其能量转化效率可高达72.47%。且该方法由于先将海水加热蒸发,海水中的绝大部分杂质不与电解槽接触,因而难以对电解槽造成破坏,因此具有良好的应用前景。
小结
目前,海水电解制氢是直接利用海水制备氢气最为成熟的技术,尽管已取得良好进展,但目前的研究仍处于早期阶段,依然面临着一些关键性挑战:
首先,对于海水电解槽,天然海水的成分复杂,如溶解的离子、细菌/微生物和杂质/沉淀物等,不可避免地导致催化剂的效率下降或对电解槽部件产生腐蚀。因此,海水的过滤/净化是直接海水电解所必需的。
其次,HER和OER电催化剂的长期耐久性也是具有挑战性的任务之一,因为活性位点在海水裂解过程中易中毒或被堵塞。在这方面,采用合适的隔膜将催化剂与海水中的离子隔离,或开发具有抗腐蚀能力的催化剂,是针对这一问题的潜在解决方案。
第三,海水电解中OER选择性受到竞争的巨大挑战。为了克服这种竞争,采用碱性海水电解质、开发具有OER选择性活性中心催化剂或在催化剂上使用氯阻挡层成为目前有效解决方案。
第四,为了深入理解海水裂解的反应机理,有必要开发先进的表征技术,如原位显微镜、光谱学和色谱法等技术。此外,迫切需要结合原位表征和理论计算对电催化剂在实际工作条件下的催化行为进行研究。
第五,目前对海水裂解的研究主要局限于实验室水平。为了满足工业规模氢气生产的要求,设计和放大用于海水电解的新型电解槽,以及开发合适的催化剂,仍需进行大量工作,借鉴工业淡水分离系统的成功经验有可能加快这一进程。
为解决以上问题,未来通过纳米工程、表界面工程、掺杂、包覆、理论计算辅助探究活性位点来开发高性能HER/OER催化剂,以及采取选择性渗透、覆盖钝化层、净化、海水蒸气等方式来避免海水离子和杂质对电解反应的干扰,以及开展海水电解制氢的放大试验将进一步促进海水电解制氢技术的发展。
